No es lo mismo Glutaminasa que Transglutaminasa
«No soy un experto en el Big Bang, pero te equivocas respecto a la Tierra. La vida nació de la Tierra, pero la vida también la cambió…. La Tierra en la que vivimos ahora es un hogar construido por la vida para sí misma. No tiene nada que ver con Dios».
Cixin Liu, El Fin de la Muerte, 2018

**Dibujos tomados de Opensea, el mercado de los populares NFTs
La demanda e interés actual por la dieta a base de vegetales (conocida ahora, por marketing, como Plant-based), así como la nueva comunidad de personas flexitarianas, ha potenciado el desarrollo de una gran variedad de alimentos de origen vegetal (plant-based foods). Este tipo de alimentos, que pueden ser usados por personas con un estilo de vida vegano (dependiendo de sus ingredientes), se diseñaron principalmente para un consumidor que está más interesado en reducir el consumo de alimentos de origen animal, más que en eliminarlos por completo de sus dietas y puede tener varios motivos para hacerlo, como por ejemplo mejorar su salud, reducir su impacto en el cambio climático, disminuir el maltrato animal, etc. De hecho, una buena parte de estos «nuevos» consumidores a base de plantas buscan alimentos con apariencia, sabor y textura lo más similar posible a los alimentos de origen animal y de ahí todo este «boom» de las hamburguesas vegetales de empresas como «Beyond Meat» e «Impossible Burger» y su implementación en franquicias como Burger King o McDonalds. De la misma manera existe también una gran innovación en el área de quesos vegetales con la finalidad de lograr alternativas en sabor, textura y funcionalidad muy similar a la de los productos lácteos. Todo esto ha llevado a la tecnología de alimentos un paso más adelante para explorar la elaboración de productos de origen animal, sin la crianza y sacrificio de animales, y por lo tanto ya es posible elaborar carne de res, pollo y pescado, así como proteínas de leche y huevo pero con origen celular o microbiano, sin animales de por medio (Upside foods, Avantmeats, The Every Company, Remilk, Alephfarms, entre otras) y haciendo uso de la tecnología de impresión en 3D para dar la forma o figura, a la cual estamos acostumbrados con los alimentos de origen animal, para disfrutar ahora de un buen corte de carne a base de plantas, células o microorganismos (Coccus)
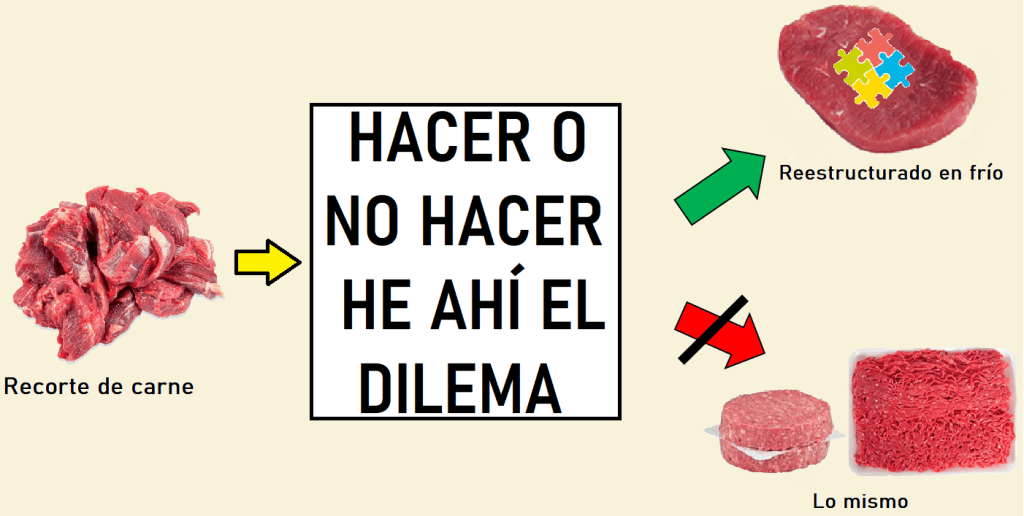
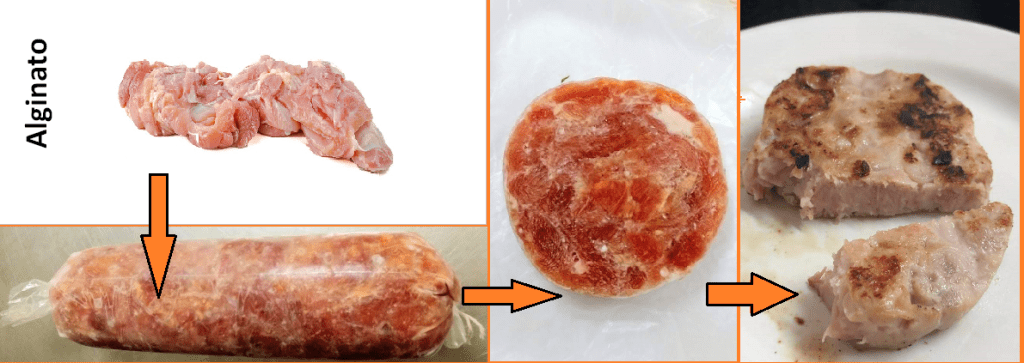
Esta revolución por crear alimentos que parezcan de origen animal está demandando, en este momento, a transformar en primer lugar las proteínas de origen vegetal en ingredientes que sean funcionales, atractivos y de gran sabor. Esto ha conducido al estudio y aplicación de diferentes enzimas en los alimentos. Algunas de las enzimas que vamos a ver continuamente en el desarrollo de alimentos a base de vegetales pertenecen a la familia de las Glutaminasas, que no tienen nada que ver con otra enzima muy conocida, de la cual hemos hablado en otros artículos, que es la Transglutaminasa (Transglutaminasa en alimentos y Valor Agregado en Carne 4).
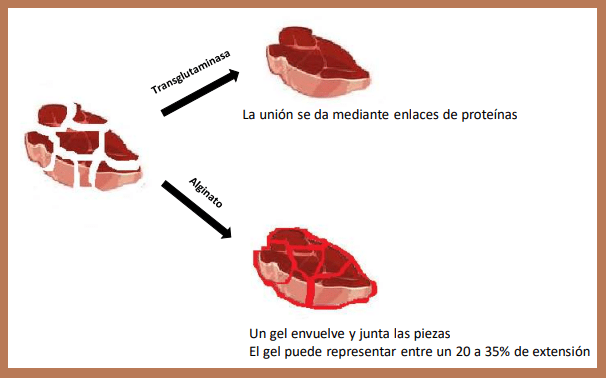
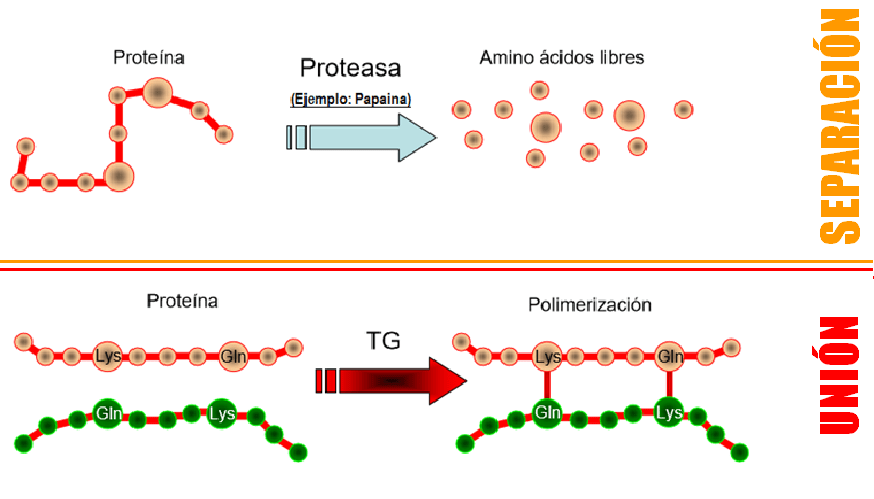
La diferencia «práctica» entre Glutaminasa y Transglutaminasa es que la primera pertenece a la familia de las hidrolasas, es decir va a hidrolizar o romper un enlace específico de los aminoácidos dentro de una proteína. En cambio la Transglutaminasa es de la familia de las transferasas y va crear enlaces covalentes específicos entre algunos aminoácidos en la proteína.
Así que hoy toca el turno de revisar brevemente los tipos de glutaminasas y su aplicación, principalmente, en el desarrollo de alimentos de origen vegetal o basados en plantas.
Proteínas
Las proteínas son esenciales en nuestra dieta, pero además de su valor nutrimental estos componentes cumplen con otras funciones cuando son utilizadas como ingredientes en los alimentos contribuyendo de esta manera a la calidad y atributos sensoriales (textura, sabor, aroma, color).
En algunos casos, el uso y aplicación de proteínas naturales (sobre todo de origen vegetal) como un ingrediente en alimentos líquidos (bebidas) no es muy fácil, dado que cuentan con poca estabilidad, funcionalidad, sabor y palatabilidad, por lo que mejorar estas características se ha vuelto muy importante para la industria alimentaria, sobre todo con la nueva tendencia de alimentos a base de plantas.
Para tener proteínas que puedan ser usadas como ingredientes funcionales (espesantes, gelificantes, emulsionantes, espumantes o ligadores de agua y grasa) es necesario modificarlas ligeramente para obtener las características o funcionalidad que deseamos. Hace aproximadamente unos 30 años, se ha utilizado con éxito la reacción de Desamidación para transformar las proteínas y ampliar su uso como ingredientes en la industria de alimentos.
Desamidación de proteínas
Es una reacción en la que grupos amida, como por ejemplo la glutamina (Gln) y la asparagina (Asn), que forman parte de las proteínas se convierten en ácidos (ácido glutámico o ácido aspártico respectivamente) con la liberación correspondiente de amoníaco. Este proceso es una herramienta muy poderosa para mejorar la solubilidad y otras propiedades funcionales de las proteínas lo que nos permite nuevas aplicaciones como ingrediente para la industria alimentaria.
La reacción puede hacerse de las siguientes maneras:
- Desamidación Química
- Ácida
- Álcalina
- Resina de intercambio iónico
- Desamidación Enzimática
- Péptido-glutaminasa
- Glutaminasa
- Proteína-glutaminasa (PG)
Para no profundizar mucho en los diferentes métodos, ya que no es el propósito del artículo, es importante señalar que en la actualidad la desamidación enzimática es preferida, sobre la química, debido a su velocidad de reacción, alta especificidad y seguridad. La desamidación química tiene varias desventajas entre ellas la hidrólisis de enlaces peptídicos y la posible formación de compuestos cuestionables para nuestra salud.
Entonces con respecto a la desamidación enzimática, es preciso mencionar que la enzima Péptido-glutaminasa no es muy utilizada en la industria ya que su uso está muy limitado a péptidos de cadena corta o de bajo peso molecular. En cambio, la enzima conocida como Proteína-glutaminasa (PG) es la más apropiada para la modificación proteica debido a que puede catalizar la reacción tanto en pequeños péptidos como en proteínas intactas o sustratos proteicos complejos (WHAT???)
Proteína-Glutaminasa (PG)
La PG es una enzima aislada de la bacteria Chryseobacterium proteolyticum y es la única que se comercializa actualmente. Es muy específica y cataliza la desamidación de los residuos de glutamina sin inducir hidrólisis u otros cambios estructurales importantes dentro de la proteína…. (WHAT DA…???) Bueno, bueno, bueno… todo esto suena demasiado técnico, así que voy a traducir que significa esto para el uso de la enzima PG en la industria de alimentos:
Cuando añadimos la enzima PG a un alimento con proteínas va a ocurrir la reacción de desamidación donde existan residuos de glutamina, la glutamina es uno de los diferentes aminoácidos que componen las proteínas. Este aminoácido se va a transformar en ácido glutámico pero sin separarse (hidrolizarse) de la proteína y sin provocarle ningún cambio estructural. Este simple hecho hace que la proteína mejore en algunas características, la más visible de ellas es el incremento en su solubilidad en agua incluso a pHs ácidos de aproximadamente 4.5. ¿Para que sirve esto? Ok, como ya habíamos mencionado anteriormente, las proteínas vegetales (sean de nueces, semillas, leguminosas o cereales) tienen varias limitantes para la elaboración de alimentos similares a los de origen animal. Así que por ejemplo cuando se mejora la solubilidad de estas proteínas es factible mejorar todas las bebidas vegetales alternativas a la leche y desarrollar además bebidas proteicas a base de frutas que requieren de una buena estabilidad a pHs bajos, evitando el problema de precipitación o asentamiento de la proteína al fondo del envase. Al mejorar la solubilidad, la enzima PG puede usarse además para elaborar suplementos de proteína vegetal en polvo que sustituyan a los suplementos de proteínas de suero de leche utilizados para preparar bebidas en casa antes de ejercitarse.
Otras modificaciones que ocurren con la desamidación de proteínas vegetales, al usar la enzima PG, son el incremento en las propiedades emulsificantes y espumantes, así como la reducción en la capacidad de gelificación y todo esto sin modificar el sabor del alimento. Estas nuevas características contribuyen por lo tanto a obtener leches vegetales más cremosas, espumosas y que no cuajan cuando se utilizan en bebidas calientes, como el café, un problema muy común que se observa en leches a base de almendras, nueces u otras semillas.
Glutaminasa
La otra enzima, que me brinqué y no he mencionado es la Glutaminasa. Esta enzima se obtiene de varios microorganismos (bacterias, hongos y levaduras) por lo que sus propiedades varían al usarse en la reacción de desamidación de proteínas. En la reacción, esta enzima es mucho más específica para modificar aminoácidos glutamina en estado libre más que como grupo residual en un péptido o en una proteína. Debido a esto, la enzima glutaminasa se utiliza comúnmente en proteínas hidrolizadas ya sea de soya, maíz, arroz, trigo para la producción de potenciadores de sabor. Cuando ocurre la desamidación, La glutamina en estado libre se transforma en ácido glutámico libre, que contribuye al sabor umami de los alimentos. El ácido glutámico es muy conocido por la mayoría de nosotros cuando se encuentra en forma de su sal con el nombre de glutamato monosódico.
El acido glutámico es un aminoácido que se encuentra de forma natural principalmente en los alimentos de origen animal (carne, pescado, lácteos) y en pocos vegetales. Dado esto, la glutaminasa puede usarse en el desarrollo de alimentos a base de plantas como una alternativa al uso directo de glutamato monosódico y que nos va a permitir imitar la nota umami presente en carnes o quesos. Comercialmente, esta enzima puede encontrarse sola o mezclada con otras enzimas dependiendo de la aplicación deseada, es decir sí se busca un perfil cárnico o lácteo.
Comentarios finales
Las enzimas de la familia glutaminasa se pueden utilizar para modificar proteínas tanto de origen animal como vegetal para modificar sus propiedades emulsificantes, espumantes, gelificación, solubilidad y sabor. En el caso específico de los alimentos a base de plantas hemos visto aquí que podemos usarlas para brindar un mejor sabor (glutaminasa) y mejorar las propiedades sensoriales en bebidas vegetales (proteína-glutaminasa).
Por otro lado, la enzima transglutaminasa puede utilizarse en alimentos vegetales que contengan proteínas para incrementar su viscosidad o mejorar la textura o firmeza en quesos vegetales.
Dos dudas existenciales
- ¿Qué pasa sí a un alimento (animal o vegetal) le añado Glutaminasa y luego quiero reestructurarlo (unirlo) con Transglutaminasa?
- ¿Qué pasa sí primero reestructuro el alimento con Transglutaminasa y luego le añado la Glutaminasa?
Escríbeme tus comentarios
** Sí quieres conocer sobre NFTs, Criptomonedas y Metaversos checa esta página: